INTOXICATION FÉLINE
Cas clinique
Auteur(s) : Martine Kammerer*, Jérôme Triffe**, Sabrina Leclerc***, Alexandra Poncet****
Fonctions :
*Centre antipoison animal
et environnemental de l’Ouest, Oniris,
BP 40706, 40307 Nantes Cedex 3
**Clinique vétérinaire du Val-des-Usses,
115, clos du Château, 74270 Frangy
***Centre antipoison animal
et environnemental de l’Ouest, Oniris,
BP 40706, 40307 Nantes Cedex 3
****Centre antipoison animal
et environnemental de l’Ouest, Oniris,
BP 40706, 40307 Nantes Cedex 3
La lipidothérapie offre de nouvelles perspectives dans le traitement de certaines intoxications.

Les médicaments, humains ou vétérinaires, représentent l’une des principales causes d’intoxication chez les animaux de compagnie. Le plus souvent, les possibilités thérapeutiques sont limitées et l’évolution peut être fatale. Cependant, un nouveau protocole se révèle très prometteur et pourrait améliorer le pronostic de ce type d’intoxications. Il s’agit de la lipidothérapie, c’est-à-dire de la perfusion d’une émulsion lipidique. Le cas rapporté ici concerne une intoxication médicamenteuse par un représentant de l’une des principales familles d’antiparasitaires potentiellement concernées, les endectocides (avermectines et milbémycines).
Un chat européen mâle âgé de 6 mois et pesant 2,9 kg reçoit en début de matinée l’application d’un antiparasitaire en spot-on, à base de moxidectine et d’imidaclopride dans sa présentation grand chien (10 à 25 kg). De trois à quatre heures plus tard apparaissent des troubles de la démarche et le chat est amené à la consultation en fin de journée, dans un état comateux. À l’examen clinique, une hypothermie (35,6 °C), une mydriase bilatérale et des myoclonies sont notées.
En raison des circonstances et des signes cliniques, l’intoxication médicamenteuse ne fait aucun doute. Le tableau clinique présenté par l’animal, assez peu spécifique, est celui qui est présent lors de surdosage par les deux antiparasitaires. Le chat a reçu une dose de 21,5 mg/kg de moxidectine et de 86 mg/kg d’imidaclopride, alors que la posologie thérapeutique est respectivement de 1 et 10 mg/kg. Les signes habituellement rapportés pour l’une et l’autre de ces molécules sont très voisins, avec une ataxie, une prostration, des tremblements, des convulsions, un coma, une mydriase et une hypersalivation. Cependant, les manifestations observées sont ici surtout liées à la moxidectine, qui est bien résorbée par la peau, alors que l’imidaclopride diffuse en surface dans le poil et n’a pu être absorbé que partiellement lors du léchage.
Si le pronostic de l’intoxication par l’imidaclopride est le plus souvent favorable, ce n’est pas toujours le cas de celle par les endectocides. Pour ces molécules, aucun antidote n’est disponible et la mise en place d’un traitement symptomatique et éliminatoire est actuellement conseillée.
Le chat reçoit donc d’abord une injection intraveineuse de diazépam (Valium®) à la posologie de 1 mg/kg, ce qui permet de faire cesser les troubles musculaires. Puis il est placé sur un tapis chauffant et sous perfusion d’une solution isotonique de chlorure de sodium (photo 1).
Le chat est hospitalisé et son propriétaire averti que le pronostic est réservé. La mise en place d’un protocole de lipidothérapie est décidée en accord avec le propriétaire car cette mesure thérapeutique a été utilisée avec succès dans le cas d’un surdosage par ces médicaments chez les carnivores. L’injection d’une émulsion lipidique à 20 % (Intralipide®) est réalisée dans le quart d’heure suivant, avec un premier bolus de 1,5 ml/kg en 10 minutes, puis sous la forme d’une perfusion lente à raison de 0,25 ml/kg/min pendant 30 minutes grâce à une pompe à perfusion. Durant la nuit, la perfusion de solution de chlorure de sodium est poursuivie. Le lendemain matin, l’état clinique de l’animal s’est sensiblement amendé, avec un retour de l’état de conscience et le rétablissement des réflexes photomoteurs, puis du réflexe de clignement à la menace. Quelques myoclonies subsistent et l’injection d’Intralipide® est renouvelée selon les mêmes modalités que la veille. L’amélioration se poursuit et le chat est rendu à son propriétaire 24 heures plus tard parfaitement rétabli (photo 2).
Plusieurs spécialités vétérinaires antiparasitaires contiennent des endectocides. Les intoxications ne sont pas rares, en raison soit d’un surdosage, soit d’une administration à des chiens porteurs d’une mutation du gène MDR1, responsable d’une augmentation de la perméabilité de la barrière hémato-méningée à certaines molécules (colleys et apparentés, bergers australiens pour ne citer que les principales races concernées). Les manifestations sont liées à un effet GABAergique. Dans son rapport d’expertise sur les effets indésirables de la moxidectine chez les carnivores (publié en 2005 avant la mise sur le marché de spécialités destinées à ces espèces), la Commission nationale de pharmacovigilance vétérinaire mentionnait un seul cas classé comme “possible” chez le chat, après l’application d’une solution pour-on destinée aux bovins (dose inconnue) [7]. Chez le chien, 28 cas, notifiés comme probables ou possibles, ont permis de recenser les principaux signes observés, tels qu’une ataxie, une hypersalivation, des convulsions, des tremblements, un coma, une hyperesthésie et une modification du diamètre pupillaire. Trois cas se sont révélés mortels. Dans son rapport 2011 sur la pharmacovigilance vétérinaire, l’Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail (Anses) relève 28 médicaments vétérinaires qui ont donné lieu à au moins 10 “cas graves” (susceptibles de mettre la vie de l’animal en danger) [1]. Les pipettes à base de l’association moxidectine-imidaclopride destinées au chat figurent dans cette liste (cependant, la fréquence des effets indésirables graves est inférieure à 1/10 000) [1]. Les différents cas rapportés dans la littérature chez le chien montrent que l’évolution clinique peut être longue, sur plusieurs jours, voire plusieurs semaines, et parfois mortelle [4]. L’élimination est en effet très lente. Peu de données publiées pour le chat existent, mais des études cinétiques et des observations toxicologiques sont disponibles pour le chien. Un essai réalisé dans cette espèce après une administration orale unique fait état d’une demi-vie d’élimination de la moxidectine de l’ordre de 25 jours [2].
Le traitement des intoxications par les avermectines est actuellement très limité (tableau). La mesure la plus spécifique est l’administration de charbon actif, y compris lors d’application cutanée, car la moxidectine comme tous les endectocides, est éliminée par la bile et suit un cycle entéro-hépatique [15]. Mais l’emploi de ce médicament n’est pas toujours aisé. Pour atteindre la dose efficace, il convient généralement de faire appel à des formes pulvérulentes et l’administration forcée est alors difficile. Chez un animal sédaté, une sonde nasogastrique peut être utilisée. L’administration de charbon à un animal qui présente encore des vomissements est déconseillée en raison du risque de fausse déglutition. Dans notre cas, le chat n’a pas reçu de charbon car le médicament n’était pas disponible à la clinique.Il est inutile de chercher à accélérer la diurèse car l’élimination rénale est insignifiante. Lors de convulsions ou de tremblements, un anticonvulsivant comme le diazépam est recommandé. Si la voie d’exposition est cutanée, l’animal est lavé, à l’aide de liquide vaisselle de préférence, en veillant à prévenir le refroidissement. Lors de parésie ou de coma, aucun traitement spécifique ni symptomatique n’est disponible, et le vétérinaire est assez démuni.
L’information sur la dose létale expérimentale chez les carnivores domestiques n’est pas disponible, faute d’études expérimentales chez ces espèces. Dans le cas présent, la dose reçue par le jeune chat (21,5 mg/kg) n’est pas très éloignée de la DL50 per os estimée chez la souris (50 à 100 mg/kg). Cette référence, ainsi que les observations publiées ou rapportées dans le cadre de la pharmacovigilance conduisaient à un pronostic très réservé. Il est donc probable que le rétablissement relativement rapide de l’animal soit lié à la perfusion lipidique, car la dose reçue et le tableau clinique observé laissaient craindre une issue moins favorable.
L’injection d’une émulsion lipidique lors d’intoxication est une mesure thérapeutique récemment introduite en médecine humaine [11]. Ces émulsions, à base le plus souvent d’huile de soja, sont disponibles depuis 1960, avec pour indications la nutrition parentérale et la mise en solution de principes actifs liposolubles. Leur intérêt en toxicologie a été montré pour la première fois en 1998 chez le rat intoxiqué par de la bupivacaïne. D’autres essais expérimentaux ont ensuite été réalisés chez des chiens ayant reçu des doses toxiques d’un antihypertenseur, le vérapamil, et c’est en 2006 qu’a été publié le premier cas clinique chez un patient humain traité par lipidothérapie après un arrêt cardiaque à la suite d’une anesthésie locale par une association bupivacaïne/mépivacaïne [16]. Le protocole a été par la suite mis en œuvre dans des cas similaires, puis étendu au traitement de l’intoxication par d’autres médicaments, en particulier par les antidépresseurs tricycliques et les cardiotropes (β-bloquants et inhibiteurs calciques) [9].
L’utilisation de la lipidothérapie en médecine vétérinaire qui s’en est suiviea concerné d’abord la moxidectine, puis l’ivermectine et la lidocaïne. Récemment, le traitement a été mis en œuvre avec succès chez des chats intoxiqués à la perméthrine. Le protocole employé est extrapolé de celui qui a été choisi en médecine humaine, lequel a été instauré de façon empirique.
Le premier cas clinique publié en médecine vétérinaire est celui d’un jack russel âgé de 4 mois, intoxiqué à la moxidectine et présentant des convulsions, une paralysie et un coma [8]. En plus du traitement habituel, le chiot a reçu une perfusion d’émulsion lipidique à 20 %, avec un premier bolus de 2 ml/kg suivi de 4 ml/kg/h pendant 4 heures. Chez le chat, une intoxication à la lidocaïne a été traitée par l’injection d’une dose de 1,5 ml/kg, administrée sur une période de 30 minutes [13]. Pour le traitement d’une intoxication à l’ivermectine, un autre auteur a utilisé d’abord un bolus de 1,5 ml/kg, puis une perfusion de 0,25 ml/min pendant 30 minutes [14]. Cette posologie est également celle qui a été instaurée par Clarke et coll. dans le cas d’une intoxication à l’ivermectine chez un border collie, mais avec une injection lente du bolus (10 minutes) et une perfusion plus longue (1 heure) [6]. Ce protocole a également été suivi, avec ou sans bolus initial, par le service des urgences de l’université vétérinaire de Perth, en Australie, pour 3 cas distincts d’intoxication chez le chat, à la suite del’application de pipettes à base de perméthrine et de pyriproxyfène [12]. L’un des animaux a reçu ce traitement tardivement (plus de 72 heures après l’application), les 2 autres plus tôt (9 et 15 heures après). Un traitement symptomatique et éliminatoire classique a été mis en place parallèlement (propofol, méthocarbamol, charbon actif, décontamination cutanée). L’amélioration de l’état clinique des chats à la suite de la perfusion de l’émulsion lipidique a été rapide (dans les heures qui ont suivi). En raison du recul important dont fait l’objet cette intoxication, les auteurs considèrent que la lipidothérapie a sensiblement accéléré le rétablissement des animaux. Cette dernière vient également d’être tentée avec succès chez un poney intoxiqué par l’ivermectine, aux doses préconisées chez les carnivores [5].
Le protocole qui a été suivi dans le cas présenté s’est appuyé sur les premières expériences rapportées en pratique vétérinaire. Cependant, le bolus initial aurait pu être injecté sur une durée plus courte. Il semble, en effet, important de commencer par une administration rapide, avant de prendre le relais par une perfusion lente. En médecine humaine, lors d’arrêt cardiaque lié à un anesthésique local, il est conseillé d’administrer le bolus en 1 minute. L’administration peut être renouvelée selon les mêmes modalités, 12 ou 24 heures plus tard, mais il est préférable (chez l’homme) de ne pas dépasser une dose totale de 8 ml/kg. La durée totale de la perfusion n’est pas déterminée et peut être fondée sur la réponse clinique [11]. La spécialité Intralipide® est disponible en officine, en poches de 250 ml et de 500 ml (à un prix moyen d’environ 40 € et 60 € respectivement). Les poches entamées doivent être conservées au réfrigérateur et utilisées dans les 24 heures [10].
Cette perfusion ne dispense pas des autres mesures thérapeutiques. Il est donc recommandé de placer un cathéter sur chacune des veines céphaliques, l’un étant réservé à l’Intralipide®, et l’autre aux solutions aqueuses de NaCl, de glucose ou de lactate de Ringer, si besoin.
Les effets indésirables observés chez l’homme sont rares. Il s’agit tout d’abord de ceux qui sont dus à une contamination microbienne lors de l’injection, entraînant une infection systémique et une phlébite. L’injection doit donc être réalisée dans des conditions d’asepsie optimales, si possible avec des gants et des champs chirurgicaux [10]. De plus, une réaction anaphylactoïde peut exceptionnellement se produire. Elle se manifeste dans les 20 minutes qui suivent l’injection par les signes cliniques suivants : une hyperthermie, des vomissements, une dyspnée, une tachypnée et une cyanose, une arythmie et une hypotension, puis un collapsus. L’administration intraveineuse d’héparine pourrait alors être justifiée, pour réduire la concentration plasmatique en acides gras. Le risque d’embolie est nul si une émulsion dont les gouttelettes présentent un diamètre inférieur à 0,5 µm est employée, ce qui est le cas de l’Intralipide® (photo 3). L’utilisation de la lipidothérapie en médecine vétérinaire n’en est qu’à ses débuts et les animaux qui en ont fait l’objet sont trop peu nombreux pour affirmer la parfaite innocuité de ce traitement. Cependant, dans tous les cas publiés, ainsi que dans les quelques essais thérapeutiques réalisés sur le terrain et rapportés au Centre antipoison animal et environnemental de l’Ouest, la tolérance a été très bonne et aucun effet indésirable n’a été noté.
Le mécanisme d’action antitoxique des émulsions lipidiques est encore mal connu. Il pourrait être multiple [3]. Un effet sur le métabolisme du myocarde a été initialement envisagé lors d’utilisation pour une intoxication aux médicaments cardiotropes. Les lipides sont une source d’énergie, augmentent la pénétration du calcium dans la cellule, possèdent un effet vaso-actif sur les récepteurs α-adrénergiques, et réduisent la vasodilatation provoquée par le monoxyde d’azote et l’insuline. Cependant, un effet de piégeage des substances lipophiles dans un compartiment artificiellement créé dans le milieu intravasculaire est également évoqué, permettant ainsi leur extraction du système nerveux où s’exercent les effets toxiques. Ce mécanisme apparaît plus compréhensible dans le cas de la moxidectine. La mise en évidence d’une augmentation de la concentration sérique en ivermectine immédiatement après la perfusion de l’émulsion chez un chien intoxiqué est en faveur de cette hypothèse [6].
Pour ce jeune chat présenté dans le coma après un surdosage massif de moxidectine, le pronostic était très réservé et il est probable que la perfusion lipidique ait largement contribué à l’issue favorable et au rétablissement rapide de l’animal.
La lipidothérapie est une mesure thérapeutique qui pourrait se révéler prometteuse dans le traitement de diverses intoxications en médecine vétérinaire. De nouvelles données doivent encore être rassemblées afin de mieux cerner les indications et les modalités d’administration. Le protocole n’est pas arrêté, et, en médecine humaine, un site Internet consacré à cette thérapeutique recueille les observations des praticiens qui l’ont mis en œuvre(1). En médecine vétérinaire, les centres antipoison des écoles vétérinaires pourraient se charger de cette collecte.
Son intérêt a été montré lors d’intoxication par les endectocides et, plus récemment, par la perméthrine, mais il est probable que, prochainement, de nouvelles indications soient découvertes, comme l’intoxication par d’autres insecticides ou produits phytosanitaires, par les huiles essentielles, les hydrocarbures et diverses autres substances très liposolubles et lentement éliminées.
→ Il n’existe aucun antidote pour les intoxications par les endectocides. Le pronostic est réservé car ces médicaments très liposolubles sont éliminés lentement de l’organisme.
→ La lipidothérapie consiste à administrer par voie intraveineuse une émulsion lipidique à 20 % disponible en officine, selon le protocole utilisé en médecine humaine, sous forme de bolus suivi d’une perfusion de 30 minutes à 1 heure.
→ L’intérêt de la lipidothérapie reposerait sur l’extraction de l’agent toxique liposoluble vers le compartiment lipidique ainsi créé dans le milieu intravasculaire.
→ L’injection doit être réalisée dans des conditions d’asepsie optimales pour prévenir les phlébites. Aucun risque d’embolie n’est rapporté.
Nous remercions les auxiliaires spécialisées vétérinaires, Carole Guillaume et Lydia Contie, qui ont largement contribué au rétablissement de l’animal grâce au nursing et aux soins attentifs qu’elles lui ont procurés.
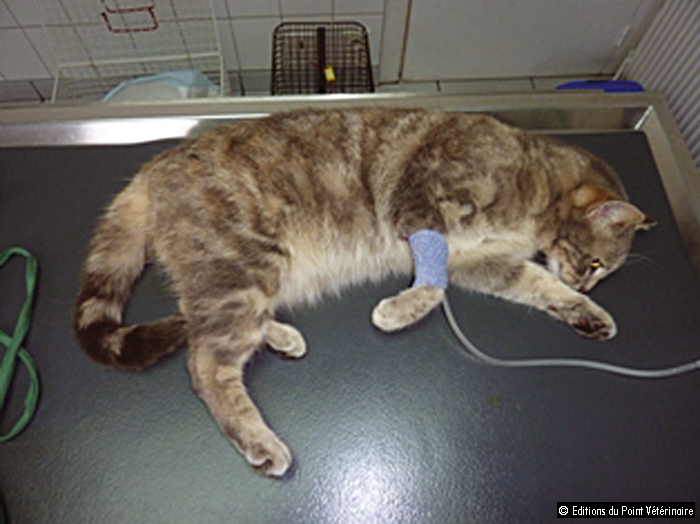
1. Après avoir reçu une injection intraveineuse de diazépam, le chat est placé sur un tapis chauffant et sous perfusion d’une solution isotonique de chlorure de sodium.
PHOTO: CAPAE-OUEST

2. En accord avec le propriétaire, un protocole de lipidothérapie est mis en place et, 24 heures plus tard, le chat est rétabli.
PHOTO: CAPAE-OUEST